Acelerando a descoberta de medicamentos: de arquivos FASTA a percepções de GenAI no Databricks
Como criar um pipeline de ponta a ponta que combina Engenharia de Dados, Modelos de Linguagem de Proteínas e GenAI na Databricks Platform.
por Ram Goli e May Merkle-Tan
- Processar dados biológicos em escala usando Lakeflow Declarative Pipelines para transformar sequências brutas de proteínas FASTA em tabelas prontas para análise no Unity Catalog.
- Classificar proteínas com modelos transformer aproveitando o ProtBERT, um modelo de linguagem de proteína, para identificar proteínas de transporte de membrana — principais alvos de medicamentos.
- Consulte query de percepções de proteínas em linguagem natural por meio de AI Functions que conectam LLMs diretamente aos seus dados, permitindo que os pesquisadores explorem candidatos a medicamentos promissores de forma conversacional.
O desenvolvimento de fármacos é notoriamente lento e caro. O ciclo de vida médio de Pesquisa e Desenvolvimento (P&D) abrange de 10 a 15 anos, com uma parte significativa dos candidatos falhando durante os ensaios clínicos. Um grande gargalo tem sido a identificação das proteínas-alvo certas no início do processo.
As proteínas são as "moléculas de trabalho" dos organismos vivos — elas catalisam reações, transportam moléculas e atuam como alvos para a maioria dos fármacos modernos. A capacidade de classificar rapidamente as proteínas, entender suas propriedades e identificar candidatos pouco pesquisados poderia acelerar drasticamente o processo de descoberta (por exemplo, Wozniak et al., 2024, Nature Chemical Biology).
É aqui que a convergência da engenharia de dados, do machine learning (ML) e da IA generativa se torna transformadora. Na verdade, você pode criar todo este pipeline em uma única plataforma: a Databricks Data Intelligence Platform.
O que estamos construindo
Nosso Acelerador de Soluções para Descoberta de Medicamentos Orientada por IA demonstra um fluxo de trabalho de ponta a ponta por meio de quatro processos principais:
- Ingestão de dados e processamento: mais de 500.000 sequências de proteínas são ingeridas e processadas do UniProt.
- Classificação por IA: um modelo transformer é usado para classificar essas proteínas como hidrossolúveis ou de transporte de membrana.
- Geração de percepções: os dados de proteínas são enriquecidos com percepções de pesquisa geradas por LLM.
- Exploração em Linguagem Natural: Todos os dados processados e enriquecidos são disponibilizados por meio de um painel e ambiente habilitados para IA que suportam consultas em linguagem natural.
Vamos percorrer cada etapa:
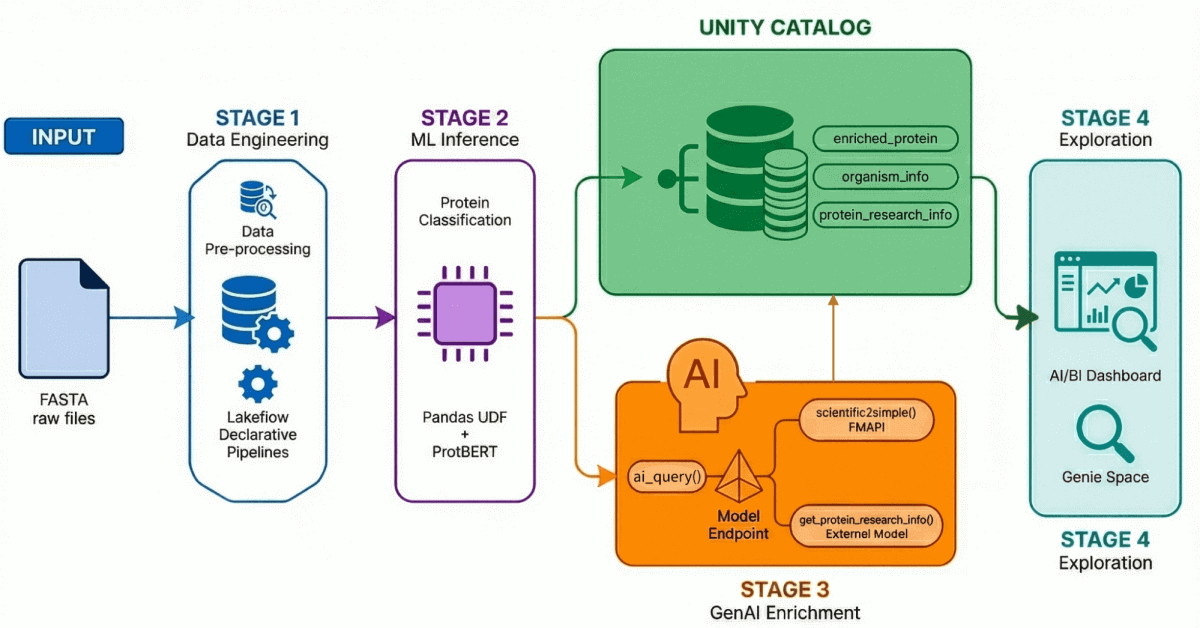
Etapa 1: Engenharia de dados com Lakeflow Declarative Pipelines
Os dados biológicos brutos raramente chegam em um formato limpo e pronto para análise. Nossos dados de origem vêm como arquivos FASTA, um formato padrão para representar sequências de proteínas que se parece com isto:
Para um olho não treinado, esses dados de sequência são quase impossíveis de interpretar: uma densa cadeia de códigos de aminoácidos de letra única. No entanto, ao final deste pipeline, os pesquisadores podem consultar esses mesmos dados em linguagem natural, fazendo perguntas como "Mostre-me proteínas de membrana pouco pesquisadas em humanos com alta confiança de classificação" e recebendo percepções acionáveis em troca.
Usando o Lakeflow Declarative Pipelines, criamos uma arquitetura medallion que refina progressivamente esses dados:
- Camada Bronze: Ingestão bruta de arquivos FASTA usando BioPython, extraindo IDs e sequências.
- Camada Prata: análise e estruturação — extraímos nomes de proteínas, informações de organismos, nomes de genes e outros metadados usando transformações regex.
- Camada Gold/Enriquecida: Dados curados e prontos para análise, enriquecidos com métricas derivadas, como peso molecular — prontos para dashboards, modelos de ML e pesquisas posteriores. Esta é a camada confiável que analistas e cientistas query diretamente.
O resultado: Dados de proteínas limpos e governados no Unity Catalog, prontos para ML e analítica posteriores. Fundamentalmente, a linhagem de dados que se estende além desta etapa para as outras (destacadas abaixo) agrega um valor incrível para a reprodutibilidade científica.
Estágio 2: classificação de proteínas com modelos Transformer
Nem todas as proteínas são iguais quando se trata da descoberta de medicamentos. Proteínas de transporte de membrana — aquelas incorporadas nas membranas celulares — são alvos de medicamentos particularmente importantes porque controlam o que entra e sai das células.
Utilizamos o ProtBERT-BFD, um modelo de linguagem de proteína baseado em BERT do Rostlab, com ajuste fino específico para a classificação de proteínas de membrana. Este modelo trata as sequências de aminoácidos como linguagem, aprendendo relações contextuais entre resíduos para prever a função da proteína.
O modelo gera uma classificação (como Membrana ou Solúvel) juntamente com uma pontuação de confiança, que gravamos de volta no Unity Catalog para filtragem e análise posteriores.
Etapa 3: Enriquecimento de dados com GenAI
A classificação nos diz o que é uma proteína. Mas os pesquisadores precisam saber por que isso importa: qual é a pesquisa recente? Onde estão as lacunas? Este é um alvo de medicamento pouco explorado?
É aqui que entram os LLMs. Utilizando tanto a API do Foundational Model do Databricks quanto os endpoints de Modelo Externo, criamos Funções de IA registradas que enriquecem os registros de proteína com contexto de pesquisa.
Etapa 4: Exploração de linguagem natural
Reunimos tudo em um dashboard de IA/BI com o Genie Space ativado.
Os pesquisadores agora podem:
- Filtrar proteínas por organismo, pontuação de classificação e tipo de proteína
- Explorar distribuições de pesos moleculares e confiança de classificação
- Faça perguntas em linguagem natural: "Mostre-me proteínas de membrana de alta confiança em humanos que são pouco pesquisadas para o tratamento do câncer"
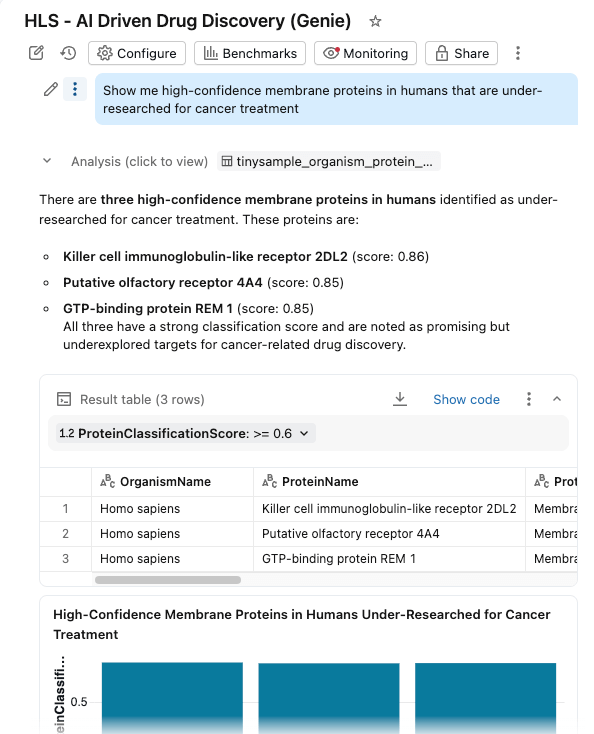
O dashboard consulta as mesmas tabelas governadas no Unity Catalog, com as AI Functions fornecendo enriquecimento sob demanda (ou processado em lotes).
O poder de uma plataforma unificada
O que torna esta solução atraente não se deve a um único componente — é o fato de que tudo roda em uma única plataforma:
| Capacidade | Recurso do Databricks |
|---|---|
| Ingestão de Dados e ETL | Pipelines Declarativos do LakeFlow |
| Governança de dados | Unity Catalog |
| Inferência de ML | GPU compute |
| Integração de LLM | FMAPI + Modelos Externos + AI Functions |
| Análises | Databricks SQL |
| Exploração | Painéis de AI/BI + AI/BI Genie Space |
Um ponto crucial �é que não há movimentação de dados entre sistemas. Sem infraestrutura de MLOps separada. Sem ferramentas de BI desconectadas. A sequência de proteína que entra no pipeline flui por transformação, classificação, enriquecimento e acaba sendo consultável em linguagem natural — tudo dentro do mesmo ambiente governado.
O acelerador de soluções completo está disponível no GitHub:
github.com/databricks-industry-solutions/ai-driven-drug-discovery
Próximos passos
Este acelerador demonstra a arte do possível. Em produção, você pode estendê-lo para:
- Processar todo o banco de dados UniProt com endpoints de taxa de transferência provisionada
- Adicionar mais modelos de classificação (abertos ou personalizados) para diferentes propriedades de proteínas
- Crie pipelines de RAG sobre literatura científica para obter respostas de LLM mais fundamentadas
- Integrar com fluxos de trabalho de simulação molecular posteriores
- Conectar à previsão da estrutura de proteínas (AlphaFold/ESMFold) para adicionar contexto estrutural 3D às proteínas classificadas
- Estenda para outros formatos genômicos (FASTQ, VCF, BAM) usando o Glow para sequenciamento em grande escala e análise de variantes
A base está lá. A plataforma é unificada. O único limite é a ciência que você deseja acelerar. Comece hoje mesmo!
(Esta publicação no blog foi traduzida utilizando ferramentas baseadas em inteligência artificial) Publicação original
Receba os posts mais recentes na sua caixa de entrada
Assine nosso blog e receba os posts mais recentes diretamente na sua caixa de entrada.